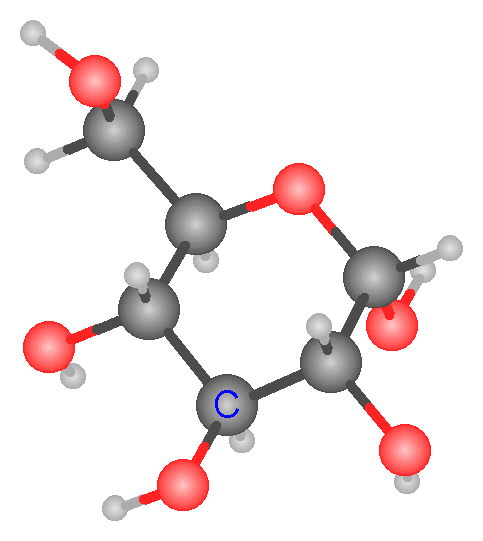
Ilmu yang mempelajari molekul disebut kimia molekuler ataupun fisika molekuler
bergantung pada fokus kajiannya. Kimia molekuler berkutat pada
hukum-hukum yang mengatur interaksi antara molekul, manakala fisika
molekuler berkutat pada hukum-hukum yang mengatur struktur dan
sifat-sifat molekul. Dalam prakteknya, perbedaan kedua ilmu tersebut
tidaklah jelas dan saling bertumpang tindih. Dalam ilmu molekuler,
sebuah molekul terdiri dari suatu sistem stabil yang terdiri dari dua
atau lebih molekul. Ion poliatomik dapat pula kadang-kadang dianggap
sebagai molekul yang bermuatan. Istilah molekul tak stabil digunakan untuk merujuk pada spesi-spesi kimia yang sangat reaktif.
Molekul didefinisikan sebagai sekelompok atom
(paling sedikit dua) yang saling berikatan dengan sangat kuat (kovalen)
dalam susunan tertentu dan bermuatan netral serta cukup stabil.[1][2] Menurut definisi ini, molekul berbeda dengan ion poliatomik. Dalam kimia organik dan biokimia, istilah molekul digunakan secara kurang kaku, sehingga molekul organik dan biomolekul bermuatan pun dianggap termasuk molekul.
Dalam teori kinetika gas, istilah molekul sering digunakan untuk merujuk pada partikel gas apapun tanpa bergantung pada komposisinya.[3]
Menurut definisi ini, atom-atom gas mulia dianggap sebagai molekul
walaupun gas-gas tersebut terdiri dari atom tunggal yang tak berikatan.[4]
Sebuah molekul dapat terdiri atom-atom yang berunsur sama (misalnya oksigen O2), ataupun terdiri dari unsur-unsur berbeda (misalnya air H2O).
Atom-atom dan kompleks yang berhubungan secara non-kovalen (misalnya
terikat oleh ikatan hidrogen dan ikatan ion) secara umum tidak dianggap
sebagai satu molekul tunggal.
1 mol adalah satuan bilangan kimia yang jumlah atom-atomnya atau
molekul-molekulnya sebesar bilangan Avogadro dan massanya = Mr senyawa
itu.
Jika bilangan Avogadro = L maka :
L = 6.023 x 1023
1 mol atom = L buah atom, massanya = Ar atom tersebut.
1 mol molekul = L buah molekul massanya = Mr molekul tersehut.
Massa 1 mol zat disebut sebagai massa molar zat
Contoh:
Berapa molekul yang terdapat dalam 20 gram NaOH ?
Jawab:
Mr NaOH = 23 + 16 + 1 = 40
mol NaOH = massa / Mr = 20 / 40 = 0.5 mol
Banyaknya molekul NaOH = 0.5 L = 0.5 x 6.023 x 1023 = 3.01 x 1023 molekul.
Download Latihan Soal KIMIA UN SMA 2010 – IPA
download soal UN kimia SMA
belajar dan terus belajar ayo belajar kimia bersama
Entri Populer
-
Dalam bentuk molekul dikenal adanya teori ikatan valensi. Teori ini menyatakan bahwa ikatan antar atom terjadi dengan cara saling bertin...
-
Sifat – Sifat Halogen X 2 Fluor (F 2 ) Klor (Cl 2 ) Brom (Br 2 ) Iodium (I 2 ) 1. Molekulnya Diatom 2. Wu...
-
Kalsium, stronsium, barium, dan radium membentuk senyawa ion bermuatan +2. Magnesium kadang-kadang bersifat kovalen dan berilium lebih d...
-
Orde reaksi atau tingkat reaksi terhadap suatu komponen merupakan pangkat dari konsentrasi komponen tersebut dalam hukum laju. Sebagai c...
-
Pada tahun 1808, Marie Francois Raoult seorang kimiawan asal Perancis melakukan percobaan mengenai tekanan uap jenuh larutan, sehingga i...
Label
- Eksponen Hidrogen (7)
- Gas Hidrogen (2)
- gas mulia (1)
- Hasil Kali Kelarutan (3)
- Hidrokarbon (9)
- Hitungan kimia (1)
- Ikatan Kimia (6)
- Kecepatan Reaksi (5)
- Kesetimbangan kimia (6)
- Kimia kelas 1 (24)
- kimia kelas 2 (51)
- kimia kelas 3 (18)
- Kimia lingkungan (1)
- Kimia Terapan Dan Terpakai (1)
- Larutan (2)
- Reaksi kimia (1)
- Reaksi Redoks Dan Elektrokimia (10)
- Sel Elektrokimia (1)
- Sifat Koligatif Larutan (4)
- Sistem Periodik Unsur-Unsur (1)
- Sistim koloid (4)
- Soal-soal kimia (1)
- Stoikiometri (4)
- Struktur Atom (5)
- Teori Asam-Basa Dan Stokiometri Larutan (2)
- Termokimia (4)
- Tokoh Penemu ilmu dan hukum kimia (1)
- Unsur-Unsur Alkali (3)
- Unsur-Unsur Alkali tanah (4)
- Unsur-unsur halogen (3)
- Unsur-Unsur Periode Ketiga (1)
- Unsur-Unsur Transisi Periode Keempat (4)
- Video (2)
- Zat Radioaktif (2)
Arsip Blog
-
▼
2011
(30)
-
▼
Desember
(30)
- Eksponen Hidrogen : Menyatakan pH Larutan Basa
- Eksponen hidrogen : Menyatakan pH Larutan Asam
- Kimia : Eksponen Hidrogen
- Larutan : Konsentrasi larutan
- Kimia : Penjelasan tentang larutan
- Kesetimbangan kimia : Kesetimbangan Disosiasi
- KESETIMBANGAN KIMIA : PENGARUH KATALISATOR TERHADA...
- Kesetimbangan kimia :Pergeseran kaesetimbangan
- Kesetimbangan kimia : Hukum kesetimbangan
- kesetimbangan kimia : Keadaan Kesetimbangan
- Kimia : Kesetimbangan kimia
- Kecepatan/Laju Reaksi : Faktor-Faktor Yang Mempeng...
- Kecepatan Reaksi : Tahap Menuju Kecepatan Reaksi
- Kecepatan reaksi : Teori Tumbukan Dan Teori Keadaa...
- Kecepatan reaksi : Orde Reaksi
- Konsentrasi Dan Kecepatan Reaksi
- Sistem koloid : Pembuatan Koloid
- Elektroferisis Dan Dialisis
- Sistem koloid : Sifat-Sifat Koloid
- Sistim koloid : Sistem Dispers Dan Sistem Koloid
- Energi dan ikatan kimia
- Penentuan Perubahan Entalpi Dan Hukum Hess
- Perubahan Entalpi
- Reaksi Eksoterm Dan Reaksi Endoterm
- Hitungan kimia
- Persamaan reaksi kimia
- Konsep mol dan pengertian molekul
- Massa Atom Dan Massa Rumus
- Hukum-Hukum Dasar Ilmu Kimia
- Jabir Ibnu Hayyan Adalah Penemu Ilmu Kimia
-
▼
Desember
(30)
-
Entri Populer
-
Dalam bentuk molekul dikenal adanya teori ikatan valensi. Teori ini menyatakan bahwa ikatan antar atom terjadi dengan cara saling bertin...
-
Sifat – Sifat Halogen X 2 Fluor (F 2 ) Klor (Cl 2 ) Brom (Br 2 ) Iodium (I 2 ) 1. Molekulnya Diatom 2. Wu...
-
Kalsium, stronsium, barium, dan radium membentuk senyawa ion bermuatan +2. Magnesium kadang-kadang bersifat kovalen dan berilium lebih d...
-
Orde reaksi atau tingkat reaksi terhadap suatu komponen merupakan pangkat dari konsentrasi komponen tersebut dalam hukum laju. Sebagai c...
-
Pada tahun 1808, Marie Francois Raoult seorang kimiawan asal Perancis melakukan percobaan mengenai tekanan uap jenuh larutan, sehingga i...
-
-
Label
- Eksponen Hidrogen (7)
- Hidrokarbon (9)
- Ikatan Kimia (6)
- Kecepatan Reaksi (5)
- Kesetimbangan kimia (6)
- Kimia kelas 1 (24)
- Larutan (2)
- Reaksi Redoks Dan Elektrokimia (10)
- Sel Elektrokimia (1)
- Sifat Koligatif Larutan (4)
- Sistim koloid (4)
- Stoikiometri (4)
- Struktur Atom (5)
- Termokimia (4)
- Unsur-Unsur Alkali tanah (4)
- kimia kelas 2 (51)
- kimia kelas 3 (18)
Copyright © 2011 ILMU KIMIA | Powered by Blogger












0 komentar:
Posting Komentar