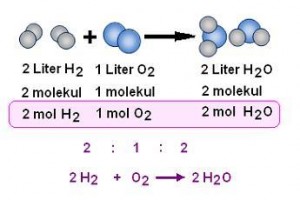
Rumus kimia pereaksi ditulis di sebelah
kiri persamaan dan rumus kimia produk dituliskan di sebelah kanan.
Koefisien yang ditulis di sebelah kiri rumus kimia sebauh zat adalah
koefisien stoikiometri, yang menggambarkan jumlah zat tersebut yang
terlibat dalam reaksi relatif terhadap zat yang lain. Persamaan reaksi
yang pertama kali dibuat oleh ahli iatrokimia Jean Beguinpada 1615.

- CH4 + 2 O2 → CO2 + 2 H2O
- 2K (s) + 2H2O (l) → 2KOH (aq) + H2 (g)
- N2(g) + 3H2(g) → 2NH3(g) ΔH = -92.4 kJ/mol.
PERSAMAAN REAKSI MEMPUNYAI SIFAT
1. Jenis unsur-unsur sebelum dan sesudah reaksi selalu sama
2. Jumlah masing-masing atom sebelum dan sesudah reaksi selalu sama
3. Perbandingan koefisien reaksi menyatakan perbandingan mol (khusus yang berwujud gas perbandingan koefisien juga menyatakan perbandingan volume asalkan suhu den tekanannya sama)
Contoh: Tentukanlah koefisien reaksi dari
HNO3 (aq) + H2S (g) ® NO (g) + S (s) + H2O (l)
Cara yang termudah untuk menentukan koefisien reaksinya adalah dengan memisalkan koefisiennya masing-masing a, b, c, d dan e sehingga:
a HNO3 + b H2S ® c NO + d S + e H2O
Berdasarkan reaksi di atas maka
atom N : a = c (sebelum dan sesudah reaksi)
atom O : 3a = c + e ® 3a = a + e ® e = 2a
atom H : a + 2b = 2e = 2(2a) = 4a ® 2b = 3a ® b = 3/2 a
atom S : b = d = 3/2 a
Maka agar terselesaikan kita ambil sembarang harga misalnya a = 2 berarti: b = d = 3, dan e = 4 sehingga persamaan reaksinya :
2 HNO3 + 3 H2S ® 2 NO + 3 S + 4 H2O
Download Latihan Soal KIMIA UN SMA 2010 – IPA
download soal UN kimia SMA












0 komentar:
Posting Komentar