|
X2
|
Fluor (F2)
|
Klor (Cl2)
|
Brom (Br2)
|
Iodium (I2)
|
| 1. Molekulnya |
Diatom
|
|||
| 2. Wujud zat (suhu kamar) |
Gas
|
Gas
|
Cair
|
Padat
|
| 3. Warna gas/uap |
Kuning muda
|
Kuning hijau
|
Coklat merah
|
Ungu
|
| 4. Pelarutnya (organik) |
CCl4, CS2
|
|||
| 5. Warna larutan (terhadap pelarut 4) |
Tak berwarna
|
Tak berwarna
|
Coklat
|
Ungu
|
| 6. Kelarutan oksidator |

(makin besar sesuai dengan arah panah)
|
|||
| 7. Kereaktifan terhadap gas H2 | ||||
| 8. Reaksi pengusiran pada senyawa halogenida |
X = Cl, Br, I
F2 + 2KX ® 2KF X2 |
X = Br dan I
Cl2 + 2KX ® 2KCl + X2 |
X = I
Br2 + KX ® 2KBr + X2 |
Tidak dapat mengusir F, Cl, Br
|
| 9. Reaksi dengan logam (M) |
2 M + nX2 ® 2MXn (n = valensi logam tertinggi)
|
|||
| 10. Dengan basa kuat MOH (dingin) |
X2 + 2MOH ® MX + MXO + H2O (auto redoks)
|
|||
| 11. Dengan basa kuat (panas) |
3X2 + 6MOH ® 5MX + MXO3 + 3H2O (auto redoks)
|
|||
| 12. Pembentukan asam oksi |
Membentuk asam oksi kecuali F
|
|||
|
Catatan : I2 larut dalam KI membentuk garam poli iodida I2 + KI ® Kl3 I2 larut terhadap alkohol coklat |
||||
Sifat Fisis
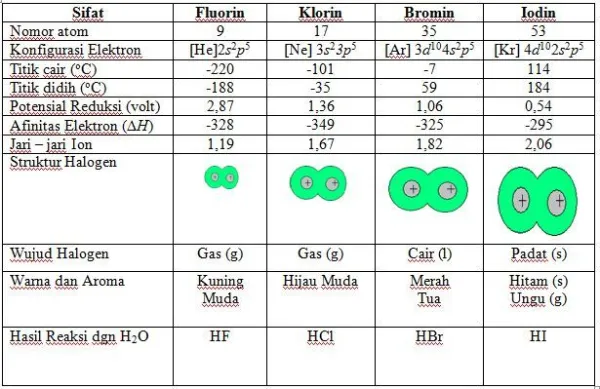
Sifat Kimia
Kereaktifan Halogen
F(g) + e F-(g) -> H = -328 kJ
Cl(g) + e Cl-(g) -> H = -349 kJ
Pada reaksi diatas kita dapat melihat, bahwa afinitas electron unsur halogen berkurang dari atas ke bawah, yaitu klorin ke iodine. Hal itu terjadi karena bertambahnya jari – jari atom, akan tetapi H (energi) fluorin lebih rendah dibandingkan klorin, penyimpangan ini terjadi karena kecilnya atom fluorin , yang membuat gaya tolak menolak antar electron.
Reaksi – reaksi pada Halogen
Halogen adalah unsur yang sangat reaktif. Unsur halogen dapat bereaksi dengan semua unsur, bahkan gas muia. Bahkan, zat yang tahan api seperti, air dan asbes dapat terbakar dalam gas fluorin.
a. Reaksi dengan logam
b. Reaksi dengan Hidrogen
c. Reaksi dengan nonlogam
d. Reaksi dengan hidrokarbon
e. Reaksi dengan air
f. Reaksi dengan basa
g. Reaksi antar halogen
Daya Oksidasi Halogen
Eo F2 = +2,87 v
Eo Cl2 = +1,36 v
Eo Br2 = +1,06 v
Eo I2 = +0,54 v
Reaksi pendesakan Halogen
F2 > Cl2 > Br2 > I2














0 komentar:
Posting Komentar