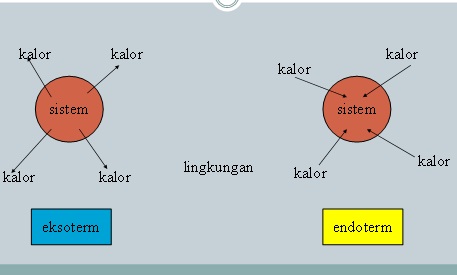
Reaksi kimia yang melepaskan atau mengeluarkan kalor disebut reaksi eksoterm, sedangkan reaksi kimia yang menyerap kalor disebut reaksi endoterm. Aliran kalor pada kedua jenis reaksi diatas dapat dilihat pada gambar 11 berikut:

Gambar 11 Aliran kalor pada reaksi eksoterm dan endoterm
Pada reaksi endoterm, sistem menyerap energi. Oleh karena itu,
entalpi sistem akan bertambah. Artinya entalpi produk (Hp) lebih besar
daripada entalpi pereaksi (Hr). Akibatnya, perubahan entalpi, merupakan
selisih antara entalpi produk dengan entalpi pereaksi (Hp -Hr) bertanda
positif. Sehingga perubahan entalpi untuk reaksi endoterm dapat
dinyatakan:ΔH = Hp- Hr > 0 (13 )
Sebaliknya, pada reaksi eksoterm , sistem membebaskan energi, sehingga entalpi sistem akan berkurang, artinya entalpi produk lebih kecil daripada entalpi pereaksi. Oleh karena itu , perubahan entalpinya bertanda negatif. Sehingga p dapat dinyatakan sebagai berikut:
ΔH = Hp- Hr < 0 ( 14 )
Perubahan entalpi pada reaksi eksoterm dan endoterm dapat dinyatakan dengan diagram tingkat energi. Seperti pada gambar 12. berikut

a.
Reaksi Eksoterm
Pada reaksi eksoterm terjadi perpindahan kalor dari sistem ke lingkungan atau pada reaksi tersebut dikeluarkan panas.
Pada reaksi eksoterm harga DH = ( – )
Contoh : C(s) + O2(g) ® CO2(g) + 393.5 kJ ; DH = -393.5 kJ
b.
Reaksi Endoterm
Pada reaksi endoterm terjadi perpindahan kalor dari lingkungan ke sistem atau pada reaksi tersebut dibutuhkan panas.
Pada reaksi endoterm harga DH = ( + )
Contoh : CaCO3(s) ® CaO(s) + CO2(g) – 178.5 kJ ; DH = +178.5 kJ
Download Latihan Soal KIMIA UN SMA 2010 – IPA
download soal UN kimia SMA












0 komentar:
Posting Komentar